Mit feinen Bläschen zu effizienteren Katalysatoren
Wie Prozesse zum Transport von grünem Wasserstoff produktiver werden
Jülich/Erlangen, 17.11.2022 – Katalysatoren sind von größter Bedeutung für die Herstellung von Chemikalien und die Energiespeicherung mit Wasserstoff. Forschende des Helmholtz-Institutes Erlangen-Nürnberg für Erneuerbare Energien (HI ERN) und der Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU) haben nun herausgefunden, dass die Bildung von Blasen in den Poren eines Katalysators sehr wesentlich für dessen Aktivität sein kann. Die Erkenntnisse helfen, Katalysatormaterialien für Reaktionen zu optimieren, bei denen aus Flüssigkeiten Gase entstehen – und die für eine künftige grüne Wasserstoffwirtschaft eine zentrale Rolle spielen.
Katalysatoren beschleunigen chemische Reaktionen, ohne dabei selbst verbraucht zu werden. Eine Vielzahl der Reaktionen in der Natur und Industrie läuft nur dank ihrer Hilfe ab. So werden Katalysatoren bei etwa 80 Prozent aller chemischen Produktionsverfahren eingesetzt und spielen auch bei Technologien zur chemischen Speicherung von Wasserstoff eine wichtige Rolle.

In den meisten Fällen handelt es sich um sogenannte heterogene Katalysatoren, die in einem anderen Aggregatzustand als die eigentlichen Reaktionspartner vorliegen. Besonders wichtig sind hier feste, poröse Katalysatoren, da diese sehr gut von flüssigen oder gasförmigen Reaktionsprodukten abgetrennt werden können.
Forschende des HI ERN und der FAU haben nun herausgefunden: Die Produktivität von Katalysatoren für Gaserzeugungsreaktionen lässt sich noch deutlich steigern, wenn sich in den Katalysatorporen besonders leicht Gasblasen bilden.

„Dieser zusätzliche Faktor, der die Reaktionsgeschwindigkeit maßgeblich bestimmt, war bislang unbekannt. Bislang ging man davon aus, dass die Geschwindigkeit nur von der chemischen Oberflächenreaktion oder vom Transport der Moleküle zu den aktiven Zentren des Katalysators bestimmt wird“, erklärt Prof. Dr. Peter Wasserscheid, Direktor des Helmholtz-Instituts Erlangen-Nürnberg, einer Außenstelle des Forschungszentrums Jülich, und Leiter des Lehrstuhls für Chemische Reaktionstechnik an der FAU.
Produktivität um Faktor 50 steigern
Die Entdeckung gelang anhand einer Reaktion, die zukünftig eine Schlüsselrolle für den Transport von grünem Wasserstoff spielen könnte. Dabei wird Wasserstoff, gebunden an ein flüssiges Trägermedium – in diesem Fall LOHC („liquid organic hydrogen carrier") gelagert und transportiert und später daraus wieder freigesetzt.
Die Technologie gilt als äußerst sicher und einfach handhabbar. Je schneller Wasserstoff aus dem Trägermedium mit Hilfe eines Katalysators wieder freigesetzt werden kann, desto kompakter und leistungsstärker kann die Technologie eingesetzt werden.
Die Forschenden des HI ERN und der FAU konnten zeigen, dass sich pro Zeiteinheit bei gleichen Bedingungen 50-mal mehr Wasserstoff aus dem Trägermedium absondert, wenn dabei die Bildung von Gasblasen in den Poren des Katalysators angeregt wird.
Die Erklärung für den enormen Unterschied: „Normalerweise produziert das System bei der katalytischen Wasserstofffreisetzung nur gelösten Wasserstoff. In der flüssigen Phase um die aktiven Zentren des Katalysators herum stellt sich dann schnell eine Sättigung ein“, erläutert Peter Wasserscheid.

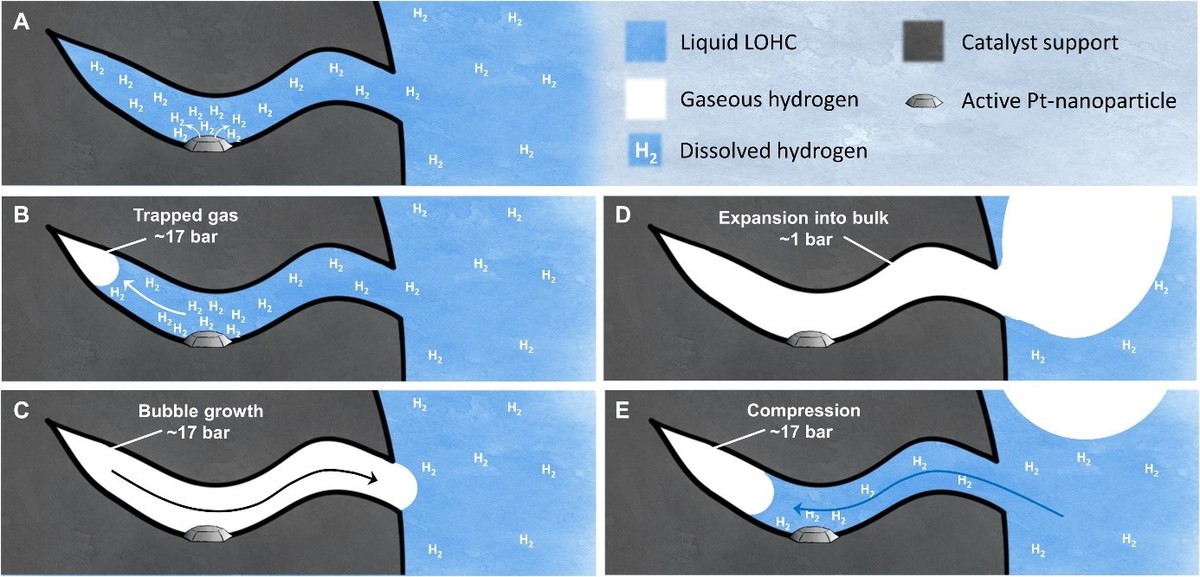
Die Bläschen in den Katalysatorporen wirken dagegen wie eine winzige Pumpe. Sie helfen, den freigesetzten Wasserstoff abzuführen. „Hat sich erst einmal eine Blase in einer Katalysatorpore gebildet, dann sammelt die wachsende Blase den gebildeten Wasserstoff ein. Wenn sich die Blase dann in die umgebende Flüssigkeit ablöst strömt der beladene Wasserstoffträger in die Pore nach und der Vorgang beginnt von vorn“, erklärt Peter Wasserscheid das Prinzip.
Experiment: Aktivierung der H2-Blasenbildung an Katalysatorpellets durch leichtes Drücken mit einem Metallstab
Die Blasenbildung, Fachbegriff: Nukleation, kann auch künstlich herbeigeführt werden; etwa indem man die Katalysatoroberfläche chemisch modifiziert oder durch einen mechanischen Reiz. Die Erkenntnisse werfen ein neues Licht auf leistungsbegrenzende Faktoren in der heterogenen Katalyse, die vor allem für die grüne Wasserstoffwirtschaft der Zukunft von sehr großer Bedeutung sind.
Die Ergebnisse wurden in Zusammenarbeit der Teams der Professoren Jens Harting, Matthias Thommes, Nicolas Vogel und Peter Wasserscheid im DFG-Sonderforschungsbereich 1452 „Catalysis at liquid interfaces“ erarbeitet und gerade in der angesehenen Zeitschrift Science Advances veröffentlicht.
Schematische Darstellung des H2-Transports mit Blasenbildung
Originalpublikation
Thomas Solymosi, Michael Geißelbrecht, Sophie Mayer, Michael Auer, Peter Leicht, Markus Terlinden, Paolo Malgaretti, Andreas Bösmann, Patrick Preuster, Jens Harting, Matthias Thommes, Nicolas Vogel, Peter Wasserscheid
Nucleation as a rate-determining step in catalytic gas generation reactions from liquid phase systems
Science Advances (16 Nov 2022), DOI: 10.1126/sciadv.ade3262
Kontakt
Prof. Dr. Peter Wasserscheid
Director and Head of Research Department Chemical Hydrogen Storage
Raum T3.94
Jessica Pölloth
PR and Communications (Parental leave)
Raum 5005


