Elektrochemische Charakterisierung
Wir entwickeln Membran-Elektrodeneinheiten vorwiegend für Protonenaustausch-Membran-Brennstoffzellen (engl. PEMFCs) und -Wasserelektrolyseure. Die hauptsächliche Auswertung dieser elektrochemischen Energieumwandler erfolgt mittels Einzelzelltests. Elektrochemische Messverfahren werden dazu verwendet, die maximale Leistung und weitere relevante Parameter wie die elektrochemisch aktive Oberfläche der Elektroden oder den Brennstoffübergang über die Membran zu bestimmen. Hier werden die charakteristischen elektrochemischen Daten von PEMFCs sowie die analytischen Werkzeuge zu ihrer Analyse vorgestellt. Die Brennstoffzelle wandelt chemische Energie aus einem Brennstoff (Wasserstoff) durch seine Oxidation zu Wasser in elektrische Energie um: Sie generiert Strom aus Wasserstoff und Sauerstoff und stößt dabei reines Wasser aus.
Polarisationsdaten
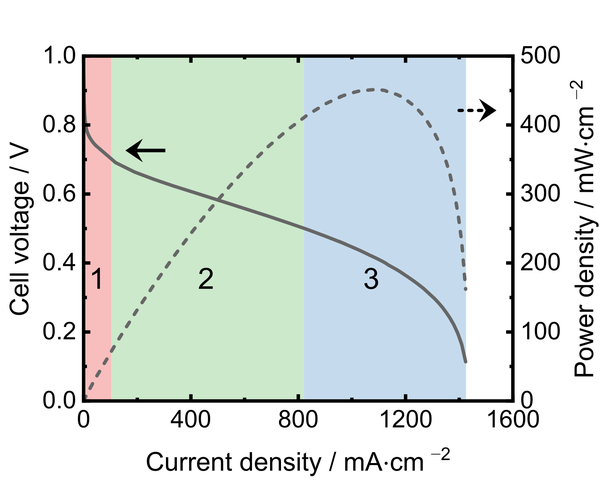
Die Polarisationskurve (U-I-Kennlinie) ist eine der gebräuchlichsten Methoden zur Charakterisierung einer Brennstoffzelle. Sie wird üblicherweise galvanostatisch aufgenommen, also durch die Entnahme konstanter Stromstärken aus der Zelle, wobei die Spannungsantwort des Systems aufgezeichnet wird. Eine wichtige Kenngröße der Polarisationskurve ist die Leerlaufspannung. Dies ist die Zellspannung, die vorliegt, wenn keine Last anliegt. Zudem kann die Polarisationskurve, wie in der Abbildung gezeigt, in drei Bereiche unterteilt werden:
- Bei niedrigen Stromdichten sinkt die Zellspannung durch Aktivierungsverluste, die mit den verwendeten Katalysatorschichten zusammenhängen.
- Bei mittleren Stromdichten sinkt die Zellspannung linear durch den ohmschen Widerstand, der hauptsächlich durch den ionischen Widerstand der Membran zustande kommt.
- Bei hohen Stromdichten tritt Konzentrationspolarisation (Massentransportverluste) auf. Sie zeigt sich in einem steilen Abfall der Zellspannung aufgrund von ungenügender Zufuhr von Gasen sowie ungenügendem Abfluss von Produktwasser.
Das Produkt aus Stromdichte und Spannung gezeigt über der Stromdichte ist die sogenannte Leistungsdichte (gestrichelte Linie in der Abbildung), die einen einfachen Vergleich von verschiedenen Brennstoffzellen ermöglicht, die mit identischen Bedingungen betrieben werden. Einzelzelltests von Brennstoffzellen werden in unseren Laboren mit 850e Testständen von Scribner Associates Inc. durchgeführt. Diese Systeme können einzelne Zellen mit einer Fläche von bis zu 25 cm² bei bis zu 180°C und mehr betreiben und ermöglichen die Software-basierte Steuerung der Gasauswahl, des Gasflusses, der Gasbefeuchtung und des Rückdrucks.
Elektrochemische Impedanzspektroskopie
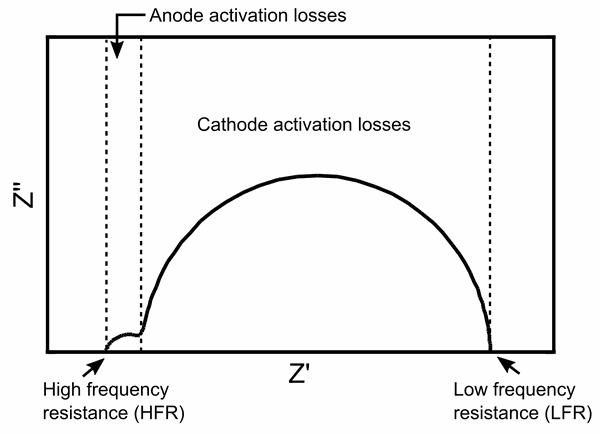
Impedanzspektroskopie ist eine Technik zur Messung der Widerstände in einer Brennstoffzelle. Beispielsweise ist der Polymerelektrolyt in einer Protonenaustausch-Membran-Brennstoffzelle ursächlich für den größten Teil ihres ohmschen Widerstands und repräsentiert den Widerstand für die Ionenleitung zwischen den Elektroden. Der Widerstand der Membran hängt von den Betriebsbedingungen ab. Deshalb ist es wichtig, Zellwiderstände während des Betriebs einer Zelle zu bestimmen.
In der elektrochemischen Impedanzspektroskopie wird der Zellwiderstand durch das Anlegen eines Wechselstromsignals zur elektrischen Last bestimmt, sodass der produzierte Gleichstrom der Zelle moduliert wird. Als Resultat kann die Intensität und Phasenverschiebung der Spannungsantwort der Zelle auf das Wechselstromsignal ausgewertet werden. Diese Daten ermöglichen einen tiefen Einblick in verschiedene Zellkomponenten, wie den ohmschen Widerstand (Hochfrequenzwiderstand in der Impedanzspektroskopie), Aktivierungsverluste und Massentransportverluste. Wir verwenden VP-300 und VSP-300 Potentiostaten von BioLogic zur Messung der Impedanzspektren einzelner Zellen.
Weitere elektrochemische Messtechniken
Zusätzliche elektrochemische Messungen einzelner Zellen ermöglichen die Bestimmung von Parametern wie dem Brennstoffübergang über die Membran oder der elektrochemisch aktiven Oberfläche einer Brennstoffzelle. Diese Messungen setzen eine Veränderung des Betriebsmodus der Zelle voraus: Anstelle des Betriebs als Brennstoffzelle (Wasserstoff und Sauerstoff) wird die Zelle mit Wasserstoff und Stickstoff betrieben.
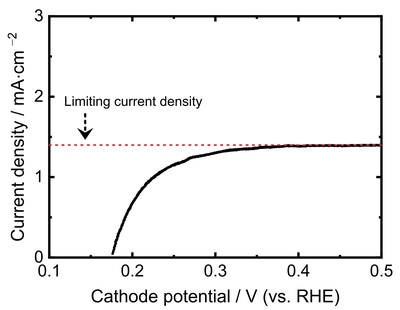
Lineare Sweep-Voltammetrie wird durchgeführt, um den Brennstoffübergang zu quantifizieren. Dabei handelt es sich um die unerwünschte Diffusion von Wasserstoff von der Anode zur Kathode der Brennstoffzelle. Der Brennstoffübergang reduziert die Effizienz der Zelle durch den Verbrauch von Wasserstoff ohne Beitrag zur Stromproduktion. Zusätzlich beschleunigt der Brennstoffübergang die Degradation einer Brennstoffzelle. Der Übergang skaliert mit der Membrandicke, hängt aber auch vom Membranmaterial ab und kann durch den Einbau von diffusionshemmenden Verstärkungsschichten in die Membran verringert werden. Wenn die Luft- oder Sauerstoffzufuhr an der Kathode durch Stickstoff ersetzt wird und eine elektrische Spannung an die Zelle angelegt wird, kann der zur Stickstoffseite diffundierte Wasserstoff elektrochemisch zurück zur Wasserstoffseite "gepumpt" werden.
Dieser Prozess ist selbstlimitierend, sobald die Wasserstoff-Pumprate gleich der Wasserstoff-Übergangsrate ist. Somit kann der Brennstoffübergang in der Brennstoffzelle bestimmt werden. Die Messung wird durch eine konstante Erhöhung der elektrischen Spannung durchgeführt, wodurch sich ihre Bezeichnung ergibt (engl. linear sweep voltammetry). Der gemessene elektrische Strom repräsentiert den Brennstoffübergang und kann mithilfe des Faradayschen Gesetzes in eine Wasserstoff-Diffusionsrate umgerechnet werden.
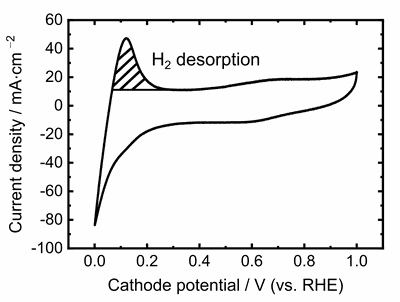
Auf einem ähnlichen Messaufbau mit Wasserstoff- und Stickstoffzufuhr zur Zelle basiert die Messung der elektrochemisch aktiven Oberfläche der Katalysatorschicht einer Brennstoffzelle. Die Zellspannung wird schnell zwischen zwei Spannungslimits erhöht und erniedrigt und die resultierende Stromantwort wird gemessen (zyklische Voltammetrie). Diese Daten ermöglichen die Berechnung der an elektrochemischen Reaktionen beteiligten Katalysatoroberfläche. Zyklische Voltammetrie kann dazu genutzt werden, um verschiedene Katalysatorschichten miteinander zu vergleichen, um Alterungseffekte zu untersuchen, oder um die Katalysatorvergiftung durch Gasverunreinigungen zu bestimmen.